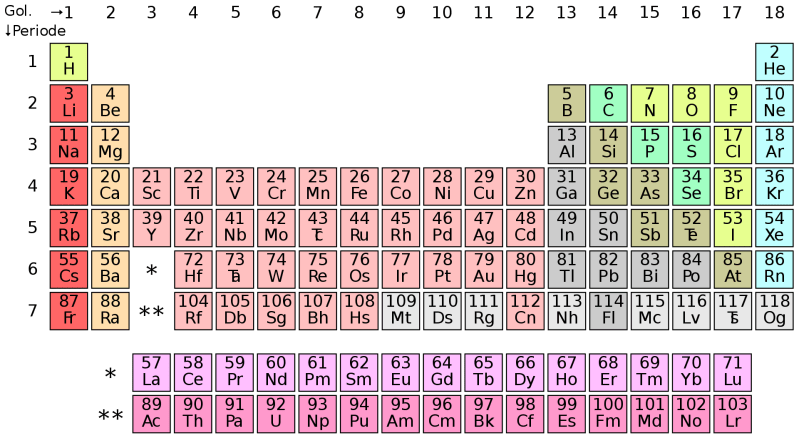
Sistem Periodik Unsur Kimia – , Jakarta Tabel periodik unsur adalah daftar unsur-unsur kimia. Unsur-unsur kimia ini didasarkan pada nomor atom (jumlah proton dalam inti atom), struktur periodik, dan sifat kimia berulang.
Tabel periodik berisi nomor atom, konfigurasi elektron, dan sifat setiap unsur. Unsur-unsur dalam tabel periodik unsur kimia terdiri dari dua golongan, yaitu golongan pertama (kolom vertikal) dan golongan kedua (kolom horizontal).
Sistem Periodik Unsur Kimia

Saat mempelajari kimia, penting untuk memahami tabel periodik unsur. Ada dua cara penamaan unsur kimia dalam tabel periodik, yaitu cara tradisional dan cara IUPAC (International Union of Pure and Applied Chemistry).
Kimia Unsur Golongan Utama Zarlaida Fitri
Seperti yang telah disebutkan sebelumnya, tabel periodik unsur kimia terdiri dari dua golongan, yaitu golongan dan periode. Kelompok berikut ada dalam tabel periodik unsur:
Dalam tabel elemen modern, grup disusun dalam kolom vertikal. Mendefinisikan suatu golongan berkaitan dengan sifat-sifat unsur tersebut. Unsur-unsur dalam suatu golongan mempunyai sifat yang serupa.
Dalam tabel periodik unsur kimia, periode disusun dalam kolom horizontal. Periode suatu unsur menyatakan jumlah kulit yang terisi elektron berdasarkan konfigurasi elektron. Tabel periodik unsur mempunyai 7 periode yaitu:
Sifat-sifat unsur. Berdasarkan sifat unsurnya, unsur dibedakan menjadi 3 jenis, yaitu logam, nonlogam, dan metaloid. Logam melepaskan elektron dari nonlogam untuk membentuk ion positif. Untuk non-logam, mereka memperoleh elektron dari logam. Hal ini berbeda dengan unsur metaloid, dimana unsur metaloid memiliki sifat logam dan nonlogam.
Sistem Periodik Unsur (spu) Serta Penjelasan Lengkap
Sinar atom. Jari-jari atom adalah jarak dari pusat atom ke orbit elektron terluar yang stabil dalam atom dalam keadaan setimbang. Jarak ini dapat diukur dalam pikometer atau angstrom. Dari atas ke bawah dalam suatu golongan, jari-jari atom bertambah seiring bertambahnya jumlah kulit elektron.
Reaktivitas. Pada tabel periodik unsur, reaktivitas meningkat dari kiri ke kanan hingga golongan VIIA.
Energi ionisasi. Energi ionisasi yang pertama adalah energi yang diserap untuk melepaskan elektron dari suatu atom. Sedangkan energi ionisasi atom lain adalah energi yang diserap untuk melepaskan elektron lain dari atom tersebut, dan seterusnya.

Afinitas elektronik. Afinitas elektron adalah energi yang dilepaskan ketika elektron berikatan dengan atom netral membentuk ion negatif. Nonlogam memiliki nilai afinitas elektron yang lebih tinggi dibandingkan logam. Dan afinitas elektron total terus meningkat sepanjang periode.
Jual Poster Tabel Periodik Unsur Kimia , Sistem Periodik Unsur Spu Klasik, Tempo Doeloe
* Fakta atau tipuan? Anda bisa menggunakan nomor cek fakta WhatsApp 0811 9787 670 dengan mengetikkan kata kunci yang diperlukan untuk mengetahui kebenaran informasi yang dibagikan, Jakarta. Bagi yang ingin belajar kimia harus mengetahui tabel periodik unsur. Secara kimia, sistem ini disebut tabel periodik. Misinya adalah menemukan nomor atom, konfigurasi elektron, dan sifat setiap unsur.
Tabel periodik unsur merupakan susunan unsur berdasarkan nomor atom dan kesamaan sifat antar unsur. Mengenali, memahami, dan menghafal reaksi kimia sangat penting untuk menghitungnya.
Mungkin terdengar rumit, namun jika sering dipraktikkan maka akan mudah diingat. Tabel periodik unsur ini dibagi menjadi tujuh kelompok.
Tabel periodik yang dirancang oleh Moseley berkembang dari waktu ke waktu sesuai dengan hukum periodik hingga mencapai bentuknya yang sekarang:
Tabel Periodik Unsur
Tabel periodik modern, seperti halnya tabel periodik panjang, memiliki kolom panjang yang disebut periode dan kolom vertikal yang disebut golongan. Dalam tabel periodik, jumlah periode ditentukan oleh 7 dan angka-angka, antara lain:
4. Periode 6 disebut periode panjang 32 unsur. Pada periode ini, unsur lantanida ditempatkan paling bawah sebagai unsur nomor 58 sampai 71.
5. Periode 7 disebut periode tidak lengkap karena jumlah faktor yang menempati periode tersebut dapat terus bertambah; Ada 24 unsur pada periode ini. Periode ini juga mencakup rangkaian unsur yang disebut deret aktinida, yaitu unsur yang diberi nomor 90 hingga 103 di bawahnya.

1984 Unsur Newlands meningkatkan berat atom. Unsur-unsur ini dapat diidentifikasi dengan nomor seri dan dibagi menjadi tujuh kelompok.
Jual Susunan Berkala Unsur Kimia Sistem Periodik Unsur Kimia
Ketujuh unsur tersebut adalah hidrogen, litium, berilium, karbon, nitrogen, boron, dan oksigen. Hubungan antara ketujuh kelompok ini dikenal sebagai aturan oktaf.
Golongan dalam tabel periodik adalah kolom vertikal tabel periodik. Kelompok dianggap penting untuk mengklasifikasikan kelompok.
Golongan dalam golongan ini adalah unsur-unsur yang susunan elektron terluarnya sama. Karena mempunyai jumlah elektron yang sama, unsur-unsur ini mempunyai sifat kimia yang mirip.
Unsur-unsur golongan pertama adalah logam dasar atau golongan dasar. Sedangkan golongan lain yang disebut logam transisi adalah logam alkali tanah. Dan dua baris di bawahnya adalah logam transisi bagian dalam, terdiri dari lantanida dan aktinida.
Tabel Periodik Unsur Kimia Bergambar Unik Ini Cocok Untuk Mahasiswa Farmasi
Sedangkan titik merupakan deret horizontal yang terdapat pada tabel periodik. Tabel periodik memiliki 7 periode, masing-masing mewakili tingkat energi suatu atom.
Tidak semua periode mempunyai jumlah unsur yang sama. dimana unsur terkecil berada pada periode 1 yang mempunyai 2 unsur. Sedangkan unsur yang paling banyak terdapat pada periode 6 sebanyak 32 unsur.
Berdasarkan sifat unsurnya, unsur dibedakan menjadi 3 jenis, yaitu logam, nonlogam, dan metaloid. Logam melepaskan elektron dari nonlogam untuk membentuk ion positif.

Untuk non-logam, mereka memperoleh elektron dari logam. Hal ini berbeda dengan unsur metaloid, dimana unsur metaloid memiliki sifat logam dan nonlogam.
Periodik Tabel (indonesian Periodic Tables Of The Elements) Michael Canov From Czech Republic
Jari-jari atom adalah jarak dari pusat atom ke orbit elektron terluar yang stabil dalam atom dalam keadaan setimbang. Jarak ini dapat diukur dalam pikometer atau angstrom.
Dari atas ke bawah dalam suatu golongan, jari-jari atom bertambah seiring bertambahnya jumlah kulit elektron.
Pada tabel periodik unsur, reaktivitas meningkat dari kiri ke kanan hingga golongan VIIA.
Energi ionisasi yang pertama adalah energi yang diserap untuk melepaskan elektron dari suatu atom. Sedangkan energi ionisasi atom lain adalah energi yang diserap untuk melepaskan elektron lain dari atom tersebut, dan seterusnya.
Mengenal Tabel Periodik Unsur Kimia Dan Penjelasan Sederhananya
Afinitas elektron adalah energi yang dilepaskan ketika elektron berikatan dengan atom netral membentuk ion negatif. Nonlogam memiliki nilai afinitas elektron yang lebih tinggi dibandingkan logam. Dan afinitas elektron total terus meningkat sepanjang periode.
Dalam sejarah perkembangannya, tabel periodik modern adalah tabel periodik modern yang diterbitkan pada tahun 1869 oleh Dmitri Mendeleev.
Sementara itu, Robert Boyle adalah orang pertama yang secara historis mendefinisikan unsur-unsur. Menurutnya, unsur adalah suatu zat yang secara kimia tidak dapat dibagi lagi menjadi dua zat atau lebih.
Setelah Boyle menjelaskan hal ini, Lavoisier menerbitkan daftar unsur-unsur, membaginya menjadi logam dan non-logam.
Sifat Periodik Unsur Kimia: Jari Jari Atom & Energi Ionisasi
Pada tahun 1869, Dmitri Ivanovich Mendeleev mengamati 63 unsur yang diketahui dan menyimpulkan bahwa sifat massa atom adalah relatif. Berdasarkan hasil pengamatannya, ia menempatkan unsur-unsur tersebut ke dalam golongan dan periode yang diketahui saat ini.
* Fakta atau tipuan? Untuk mengecek keaslian informasi yang dibagikan, Anda dapat mengirimkan nomor cek fakta 0811 9787 670 di WhatsApp dengan mengetikkan kata kunci yang diinginkan. Tabel periodik adalah tabel yang mencantumkan setiap unsur kimia dalam setiap sistem. Ada banyak unsur kimia yang mempunyai sifat berbeda antara satu unsur dengan unsur lainnya.
Saya membawa kelas
Dalam kelompok tabel periodik, sifat fisik dan kimia setiap unsur direpresentasikan sebagai sistem kimia unsur.
Sudah Hafal Lagu
Fungsi tabel periodik unsur adalah membantu mencari nomor atom dan struktur elektronik serta mempelajari sifat dan keteraturan setiap unsur.
Dalam tabel periodik, Anda akan menemukan kelompok kolom dan periode. Golongan adalah kolom vertikal atau baris vertikal dalam tabel periodik. Sedangkan titik merupakan barisan atau barisan yang mendatar.
Pengelompokan elemen berdasarkan sifat serupa telah berkembang dari yang paling sederhana hingga yang paling canggih. Dimulai dari Antoine Lavoisier, sebelum ahli kimia Inggris Henry Moseley menemukan cara menentukan nomor atom.

Buku Kimia karya Nana Sutrasna menjelaskan bahwa pada tahun 1913 Moseley melakukan eksperimen mengukur panjang gelombang unsur dengan menggunakan sinar-X.
Jual Tabel Periodik Unsur Kimia
Eksperimen Moseley menyimpulkan bahwa sifat-sifat unsur tidak bergantung pada massa atom relatifnya, melainkan pada jumlah protonnya, sehingga menghasilkan unsur-unsur dengan massa atom berbeda tetapi jumlah proton berbeda, yang disebut isotop. .
Peningkatan jumlah proton ini menunjukkan peningkatan nomor atom suatu unsur. Jadi, sifat-sifat unsur merupakan fungsi periodik dari nomor atomnya.
Tabel periodik saat ini memiliki 7 periode. Periode tersebut terbagi menjadi 2 jenis yaitu periode panjang (4, 5, 6 dan 7) dan periode pendek (1, 2 dan 3).
Jumlah golongan pada tabel periodik terdiri dari 8 golongan utama (golongan A) dan 8 golongan samping (golongan B). Unsur golongan B disebut unsur transisi. Unsur golongan B terletak pada golongan IIA dan IIIA.
Unduh Tabel Periodik Unsur Kimia Off Di Pc
Dalam tabel periodik, Anda akan menemukan bilangan dengan keteraturan sifat dasar berdasarkan jari-jari atom, keelektronegatifan, energi ionisasi, logam dan nonlogam, serta afinitas elektron.
Jari-jari atom adalah jarak dari pusat atom ke kulit terluar atom. Jari-jari atom suatu golongan akan bertambah dari atas ke bawah seiring berjalannya waktu. Hal ini disebabkan oleh bertambahnya nomor atom dan kulit elektron suatu golongan.
Seiring waktu, jari-jari atom berkurang dari kiri ke kanan, begitu pula muatan inti efektif. Semakin besar jumlah proton dalam muatan inti efektif, semakin besar daya tarik inti terhadap elektron terluar.

Ionisasi Ya
Lagu Sistem Periodik Unsur Yeni & Sayyidah
Tabel sistem periodik unsur kimia, tabel unsur periodik kimia, sistem periodik unsur kimia pdf, gambar sistem periodik unsur kimia, unsur periodik kimia lengkap, gambar unsur periodik kimia, periodik unsur-unsur kimia, susunan periodik unsur kimia, kimia sistem periodik unsur, sistem periodik unsur kimia lengkap, materi kimia sistem periodik unsur, daftar periodik unsur kimia